Vnitřní energie reálného plynu na rozdíl od ideálního plynu závisí jak na teplotě, tak i na objemu plynu. Tuto skutečnost dokazuje Joule–Thomsonův jev. Nastává při protlačování reálného plynu v tepelně izolované trubici přes pórovitou zátku.
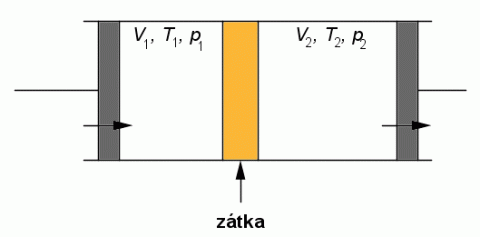
Trubice s plynem a škrtící zátkou – k vysvětlení Joule-Thomsonova jevu.
Zdroj: Techmania Science Center. Autor: Magda Králová. Under Creative Commons.
Tlak p1 větší než p2 způsobí protlačení plynu přes škrtící zátku, jejíž pórovitá struktura způsobuje škrcení plynu, takže nevzniká vírové proudění a také rychlost proudění je malá. Při ustáleném proudění můžeme pozorovat, že plyn při expanzi přes zátku bude mít na obou stranách zátky různé teploty. Jev, při kterém plyn při expanzi přes zátku mění teplotu při změně objemu se nazývá Joule–Thomsonův jev.
Experimentálně bylo zjištěno, že všechny reálné plyny se při dostatečně vysokých teplotách při Joule–Thomsonově procesu ohřívají (T2 > T1), při dostatečně nízkých teplotách (a ne příliš vysokých tlacích) se ochlazují (T2 < T1). Existuje tzv. inverzní teplota, při které je T1 = T2. Inverzní teplota závisí na druhu plynu a tlaku, např. pro vodík je to asi -80 °C (nad touto teplotou se expandující vodík zahřívá, pod ní se ochlazuje), pro helium je tato teplota asi -258 °C, pro vzduch, kyslík a dusík je to několik set stupňů celsia.
